Корженко Роман
Науковий керівник – О. М. Царенко
Кіровоградський державний педагогічний університет
імені Володимира Винниченка
Анотація. Вданій статті розглядаються особливості використання методів молекулярної спектроскопії на основі основного закону світлопоглинання. Визначено обмеження використання даного закону та умови його застосування.
Ключові слова: фотометрія, закон поглинання світла, фотоколориметр, світлофільтр.
Актуальність проблеми. Сучасний стан науки та техніки ставить певні вимоги для задоволення яких стає замало класичних хімічних методів аналізу, – це досить висока точність у порівняно короткі терміни, що дозволяє судити про склад сировини, про ступінь хімічної переробки і т.д., дає можливість активно вмішуватися в хід технологічного процесу, вводити необхідні корективи, а це, в свою чергу, дає значний економічний ефект, знижуючи енергетичні та інші затрати. Серед методів, що задовольняють дані вимоги виділяють методи молекулярної спектроскопії, так як з їх допомогою можна визначати майже усі хімічні елементи [1].
Мета дослідження. Розглянути суть роботи методів молекулярної спектроскопії на підставі основного закону світлопоглинання та з використанням фотоколориметра провести дослідження забрудненості води в річці Інгул солями важких металів.
Виклад основного матеріалу. При проходженні світла через речовину заряджені частинки речовини починають здійснювати вимушені коливання під дією електричного поля світлової хвилі. Енергія електромагнітної хвилі витрачається на збудження коливань, частково повертається у вигляді випромінювання вторинних хвиль, а частково переходить у внутрішню енергію речовини. Інтенсивність світла при цьому зменшується – відбувається поглинання світла.
Методи аналізу, котрі базуються на поглинанні енергії світла молекулами речовини складають групу абсорбційних оптичних методів, що широко використовуються на практиці. Залежно від типу частинок, що поглинають та способу трансформування енергії збудження розрізняють: атомно-абсорбційний аналіз, турбідиметрію, нефелометрію, молекулярний абсорбційний (спектрофотометрія, фотометрія, ІЧ-спектроскопія) та люмінесцентний аналіз. Останні два методи об’єднують в одну групу – методи молекулярної спектроскопії [2].
Широке застосування методів молекулярної спектроскопії в аналітичній практиці обумовлено такими важливими особливостями:
а) широкий асортимент методів (розроблено серії методик для визначення переважної більшості металів та неметалів, а також ряду органічних сполук);
б) висока чутливість (можливість визначення ряду сполук на рівні концентрацій 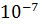 моль/л) та вибірковість визначення;
моль/л) та вибірковість визначення;
в) задовільна точність аналізу мікрокомпонентів (відносна похибка визначення зазвичай не перевищує 1–3 %);
г) не висока вартість обладнання та простота у виконанні аналізу;
д) можливість автоматизації вимірювання та застосування для безперервного контролю забруднення повітря та води, а також контролю промислових процесів.
Здатність поглинати (абсорбувати) передусім залежить від природи речовини та концентрації і може бути використана для її визначення. На цьому ґрунтуються фотометричні методи аналізу. З оптичних методів аналізу вони є найпоширенішими, тому що з їх допомогою можна визначати майже усі хімічні елементи.
Кількісна залежність поглинання світла від природи речовини і концентрації забарвленого розчину виражається законом світлопоглинання. Відомо, що закон Бугера–Ламберта–Бера (основний закон світлопоглинання) пов’язує зменшення інтенсивності світла, що пройшло крізь шар поглинаючої речовини з певною концентрацією речовини та товщиною шару: пучок монохроматичного світла інтенсивністю I0, пройшовши через шар поглинаючої речовини товщиною l, виходить послабленим до інтенсивності I, яка визначається з виразу:
 ,
,
де kλ – показник поглинання – коефіцієнт, що характеризує властивості речовини. kλзалежить від довжини хвилі λ, що поглинається світлом, і ця залежність називається спектром поглинання речовини.
Для проведення фотометричних досліджень необхідним є створення спеціальних умов (вибір світлофільтра, вибір довжини хвилі, оптична густина світлопропускання, товщина світлопоглинаючого шару та ін.).
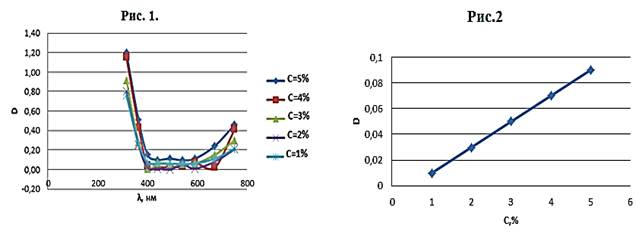
Для дослідження розчинів мідного купросу нами використано відомий метод градуювального графіка. Для цього за відомими методиками приготовлено водні розчини CuSO4 пʼяти різних концентрацій та досліджено їх з допомогою промислового фотоколориметра КФК-2. Це дало можливість побудувати спектральну криву оптичної густини для кожної концентрації (рис.1) та встановити діапазон довжин хвиль, де оптична густина мало залежить від довжини хвилі (для мідного купоросу це 490 нм).
Далі з області кожної концентрації виділяється точка з максимальним поглинанням і будується сам градуювальний графік (рис. 2), за яким можна визначати невідому концентрацію аналогічного розчину.
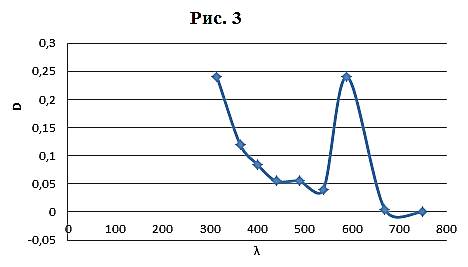
Як видно область найбільшого поглинання річкової води вкладається в межі максимального поглинання досліджених розчинів (400-600 нм), а концентрація сульфату міді в ній складає 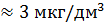 , що не перевищує гранично допустиму норму, затверджену [5].
, що не перевищує гранично допустиму норму, затверджену [5].
Висновки. Використовуючи фотоколориметричний аналіз проведено дослідження води річки Інгул на вміст у ній сульфату міді. Даний метод є перспективним експрес-методом для встановлення концентрацій відомих сполук у різних за природою розчинах.
Список літератури
- Бабко А.К., Пилипенко А.Т.. Фотометрический анализ. Определение неметаллов. - М., 1972.
- Бабко А.К., Пилипенко А.Т. Фотометрический анализ. Общие сведение и аппаратура. – М., 1968.
- http://www.eco.com.ua/sites/eco.com.ua/files/lib1/konf/3vze/zb_m/t1/tom_1_s02_p_198_201.pdf
- http://plagiatik.at.ua/publ/referati/khimija/referat_na_temu_osoblivosti_formuvannja_khimichnogo_skladu_poverkhnevikh_vod_ukrajini_u_2000_r/73-1-0-5556
- Загальний перелік ГДК і ОБРВ шкідливих речовин для води рибогосподарських водойм (№ 12-04-11 від 09.08.1990).

Коментарі